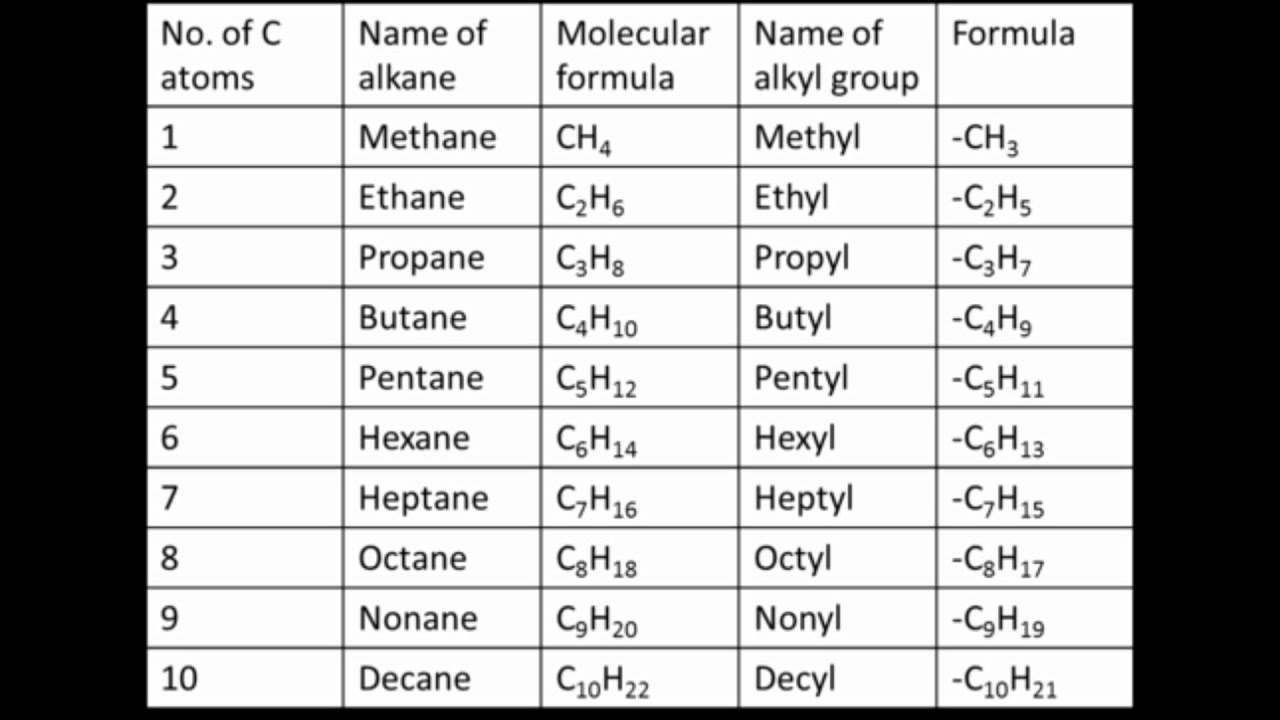
1.5 Homologe Reihe der Alkane. ( homo = gleich, logos = Stoff ) Allgemeine Summenformel der homologe Reihe. C n H 2n+2. wichtigste Eigenschaften: brennbar (bei vollständiger Verbrennung entsteht CO 2 und H 2 O) Dichte (g/cm³) kleiner als 1. in Wasser lösen sich die Alkane nicht (evtl. in Spuren), Alkane sind untereinander in jedem.. Homologe Reihe der Alkene - Chemie: Alkene sind ungesättigte Kohlenwasserstoffe mit mindestens einer Doppelbindung. Erfahrt, wie sich die homologe Reihe der Alkene über eine allgemeine Summenformel bildet und welche Eigenschaften sie besitzen. Interessiert? Dies und vieles mehr findet ihr im folgenden Text!
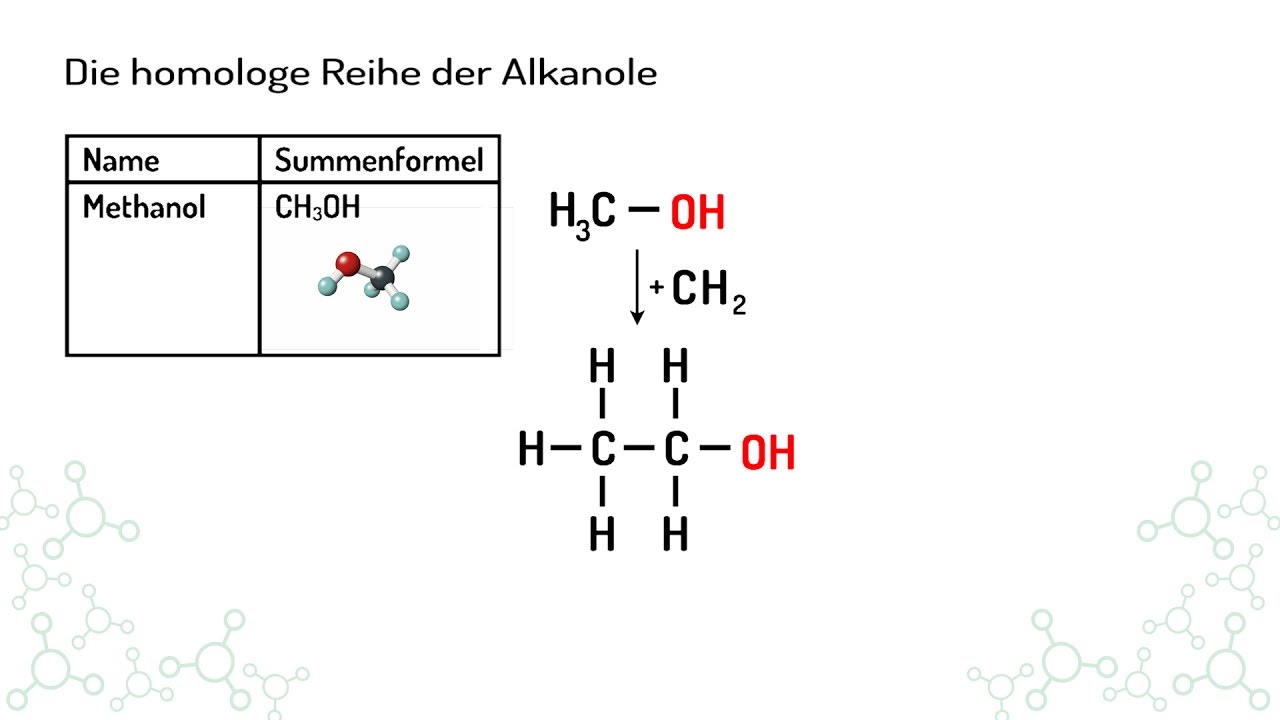
Die homologe Reihe der Alkanole (Vorschau) YouTube

02_Alkane Homologe Reihe der Alkane YouTube

Die Homologe Reihe Alkane Einfach Erklärt 9 Klasse Chemie

Die Homologe Reihe Der Alkane Tabelle gahayubild

Lernpfad zur IUPACNomenklatur der Alkane Medienbildung
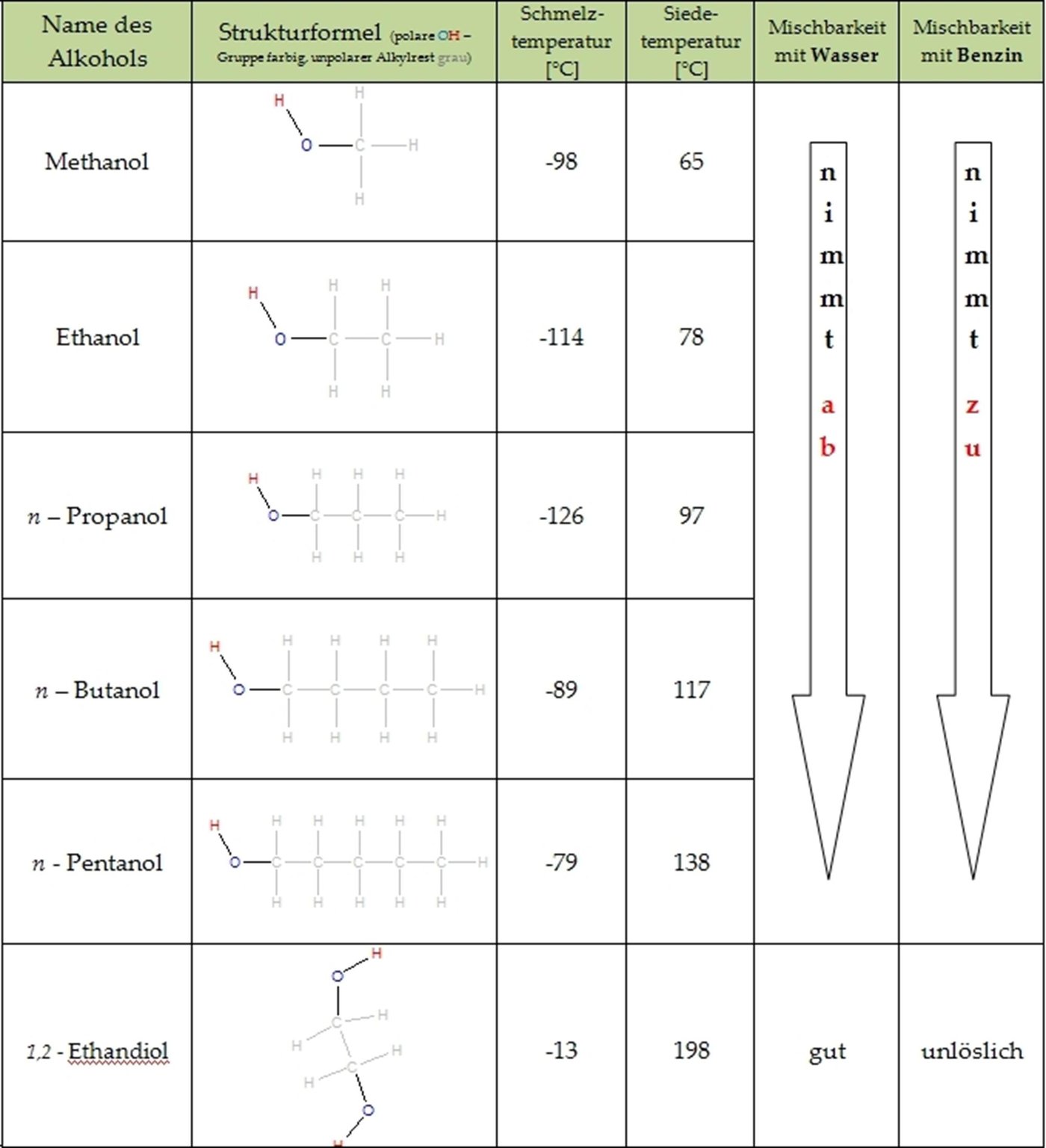
Die Homologe Reihe Der Alkane Tabelle manjahitslow
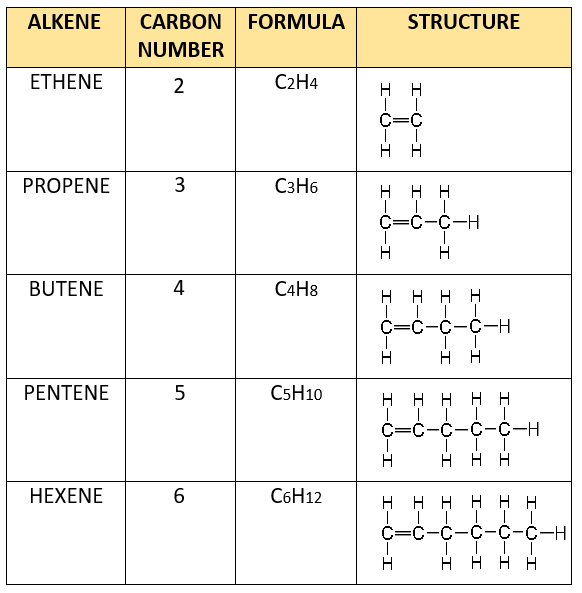
Alkenes Free Exam Academy

Homologe Reihe der Alkane YouTube

Alkane I Homologe Reihe und Benennung YouTube

Kopiervorlage Homologe Reihe der Alkane Unterrichtsmaterial im Fach Chemie Ciencias
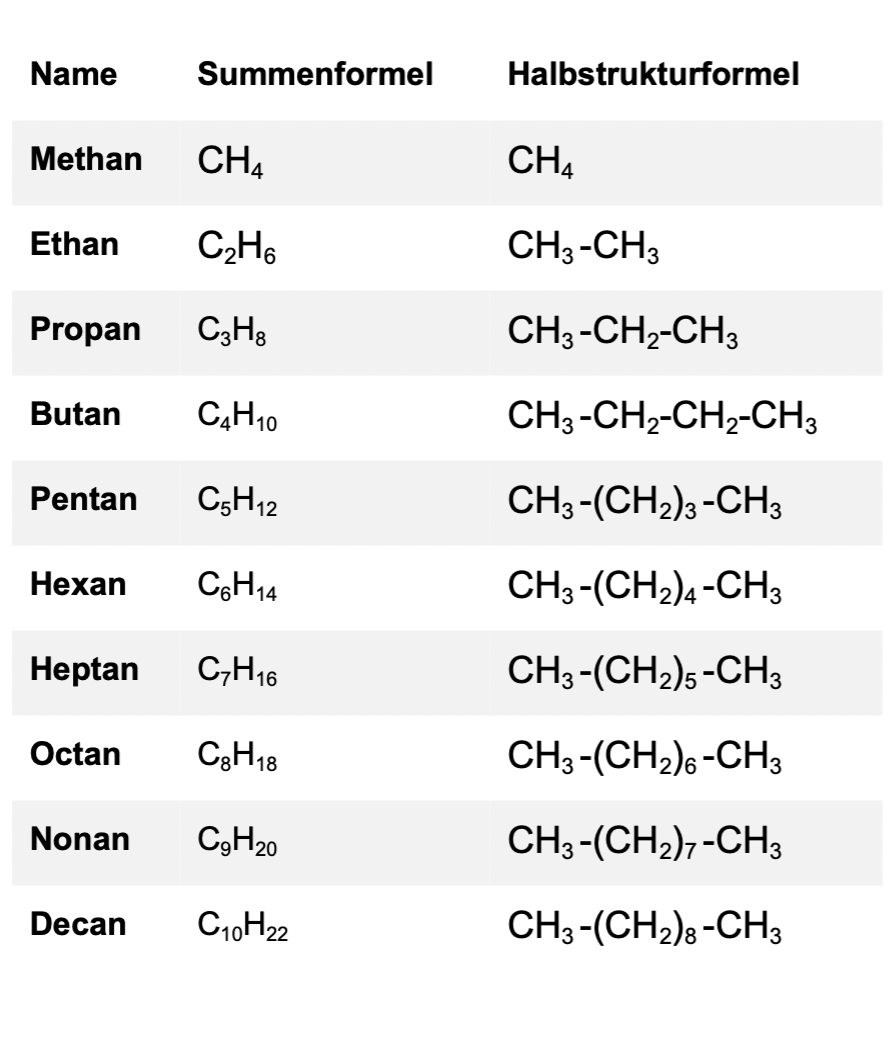
Alkane Zusammengefasst in 7 Punkte
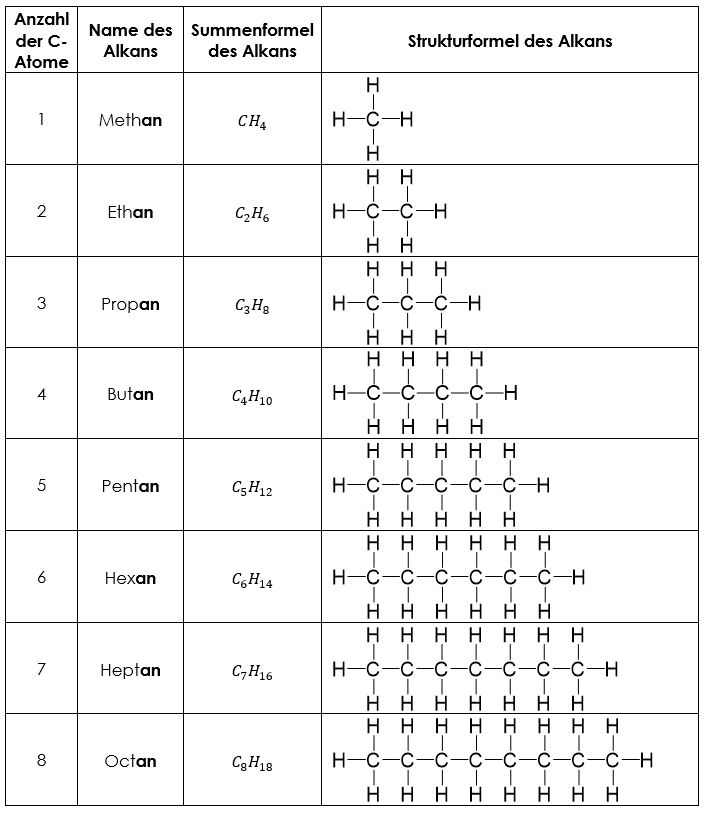
Neu Homologe Reihe Der Alkane Siedetemperatur
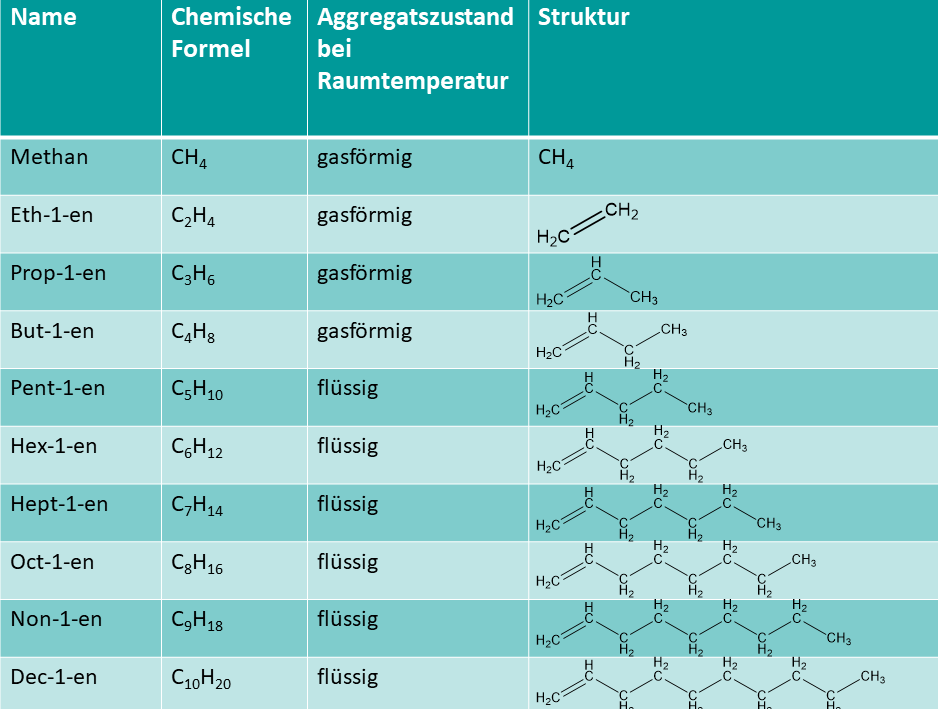
Alkene lernen mit Serlo!
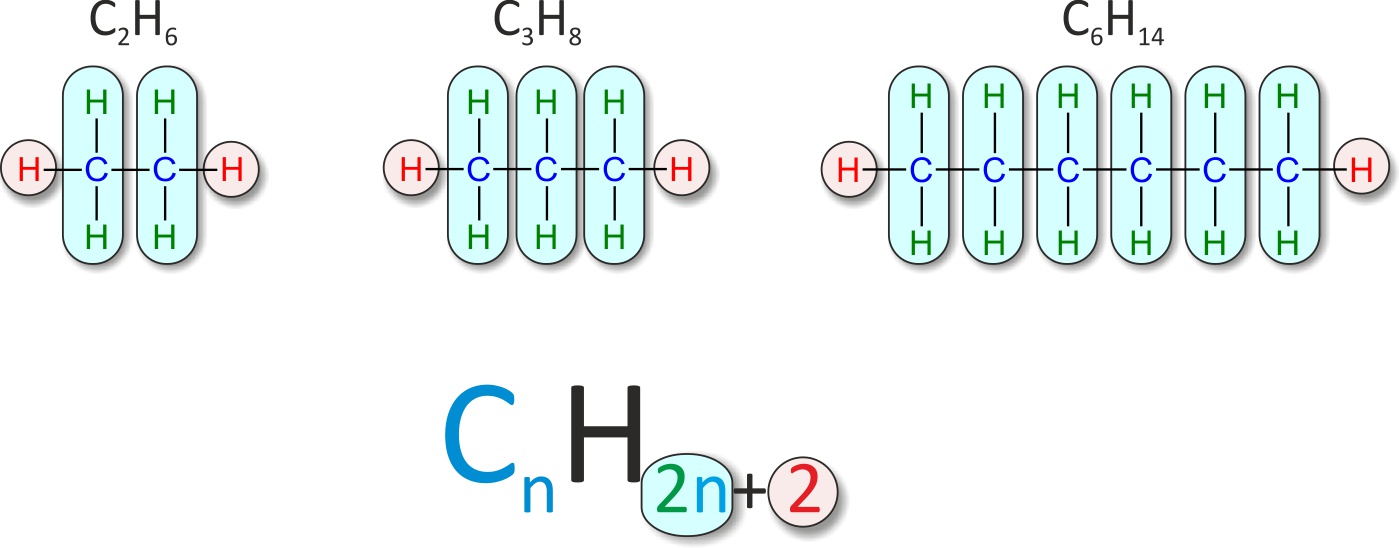
1.5 Homologe Reihe der Alkane

Die Alkane YouTube
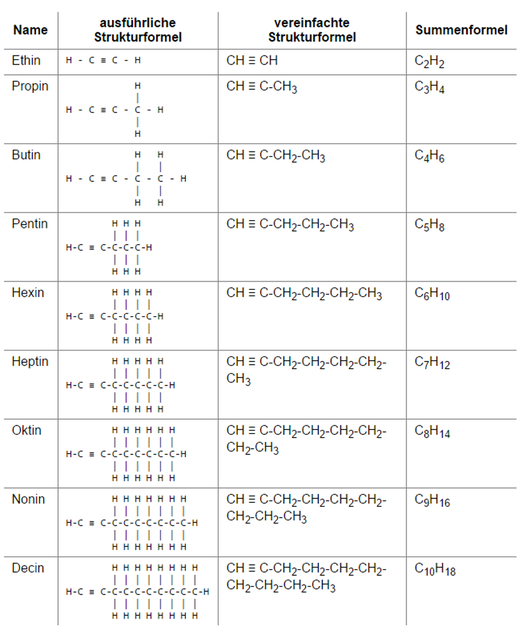
Alkane, Alkene, Alkine Vorbereitung auf den MSA
Chemistry Alkane Song YouTube
![Homologe Reihe • einfach erklärt, Überblick · [mit Video] Homologe Reihe • einfach erklärt, Überblick · [mit Video]](https://d3f6gjnauy613m.cloudfront.net/system/production/videos/004/159/bf6158b2dd8f3383db7a4adfd669b983335c2f8e/Thumbnail_Homologe_Reihe.png?1665554996)
Homologe Reihe • einfach erklärt, Überblick · [mit Video]
![Homologe Reihe • einfach erklärt, Überblick · [mit Video] Homologe Reihe • einfach erklärt, Überblick · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/02_homologe-Reihe-der-Alkohole-2-1024x576.jpg)
Homologe Reihe • einfach erklärt, Überblick · [mit Video]
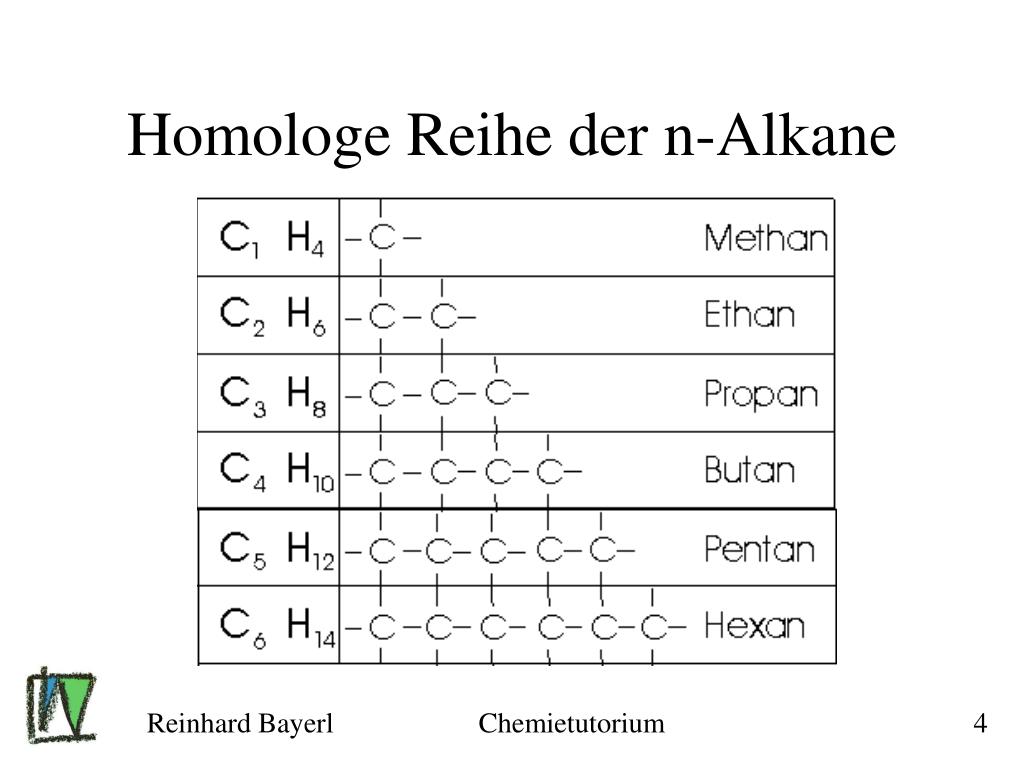
PPT Chemietutorium PowerPoint Presentation, free download ID978155
Die Werte für jeden einzelnen Stoff bzw. jeder einzelner Verbindung sind Tabellen zu entnehmen. Elemente, die in ihrer Grundform vorkommen, haben die Enthalpie 0 kJ · mol -1. (Standardbildungsenthalpie = SBE) ∆HR = Reaktionsenthalpie = Σ(∆Hf 0 Produktseite) - Σ(∆Hf 0 Eduktseite) C2H4 + 3O2 Æ 2CO2 + 2H2O. +52 0 -393 -242.. Alkine sind neben den Alkenen aliphatische und ungesättigte Kohlenwasserstoffe. Ethin ist das einfachste Alkin und damit das erste aus der homologen Reihe.Die typischen Reaktionen sind vor allem Additionsreaktionen.Eine Besonderheit stellt die CH-Acidität dar im Vergleich zu den Alkanen und Alkenen.Alkine lassen sich außerdem durch eine allgemeine Summenformel darstellen, wobei sie 2.